Scleroza sistemică: ghid complet
Redactor specializat
Biochimist, psihoterapeut, formare nutriție și terapii complementare
Studii: Facultatea de Biologie și Masterul în Biochimie.
Alte formări: cursuri acreditate de Lucrător Social, Manager proiect și Antreprenoriat, Hipnoză Clinică, Relaxare și Terapie Ericksoniană.
Scleroza sistemică, denumită și sclerodermia sistemică sau scleroza sistemică progresivă este o boală reumatică autoimună caracterizată prin producția și acumularea excesivă de colagen, numită fibroză, la nivelul pielii și al organelor interne și prin leziuni ale arterelor mici. Există două subgrupe majore de scleroză sistemică bazate pe gradul de afectare a pielii:
- Scleroza sistemică limitată
- Scleroza sistemică difuză.
Forma limitată afectează zonele de dedesubt, dar nu de deasupra, ale coatelor și genunchilor, cu sau fără implicarea feței. Forma difuză afectează și pielea de deasupra coatelor și genunchilor și se poate extinde și la trunchi.
Organele interne, inclusiv rinichii, inima, plămânii și tractul gastrointestinal pot fi afectate, de asemenea, de procesul fibrotic. Prognosticul este determinat de forma bolii și de amploarea implicării viscerale. Pacienții cu scleroză sistemică limitată au un prognostic mai bun decât cei cu formă difuză. Moartea este cauzată, cel mai adesea de afectarea plămânilor, a inimii și a rinichilor. Riscul de cancer poate fi crescut la pacienții care suferă de scleroză sistemică.
”Sclerodermia (scleroza sistemică) este o boală cronică rară, progresivă, autoimună, care afectează aproximativ 2,5 milioane de persoane la nivel mondial. Se caracterizează prin fibroză difuză și anomalii vasculare la nivelul pielii, articulațiilor și organelor interne (mai ales esofag, tract gastro-intestinal inferior, plămâni, inimă, rinichi). Boala afectează de 4 ori mai frecvent femeile decât bărbații, și este mai frecventă la grupa de vârstă 20-50 de ani.”, precizează dr. Carmina Georgescu în cadrul unui articol de pe raportuldegarda.ro
Ratele de supraviețuire în scleroza sistemică au crescut foarte mult în ultima perioadă, prin dezvoltarea unor tratamente eficiente pentru insuficiența renală. Terapiile includ medicamente imunosupresoare și, în unele cazuri, glucocorticoizi.
Articolul prezent constituie un Ghid de prezentare a sclerozei sistemice, abordând etiologia, patogeneza, simptomatologia, diagnosticul și tratamentul acestei boli grave.
Profil scleroza sistemică
În 1753, Carlo Curzio a descris primul caz de sclerodermie, care s-a considerat mai târziu a fi un scleroedem. Cuvântul „sclerodermie” a fost folosit pentru prima dată în 1836, pentru a descrie modificările pielii la un adult de către medicul milanez Fantonetti. Modificările vasospastice trifazice au fost descrise pentru întâia oară de Maurice Raynaud în 1862. Natura sistemică a bolii, cu afectare pulmonară și/sau renală crescută și mortalitate mare a fost descrisă în 1894 în manualul Principiile și practica medicinei de Osler. Sindromul Thibierge-Weissenbach a fost descris în 1910, fiind ulterior descris ca sindrom CRST de Winterbauer, în 1964.
Deși s-au înregistrat progrese importante în înțelegerea fiziopatologiei sclerodermiei în ultimii câțiva ani, boala prezintă o încă morbiditate și mortalitate semnificative. Această afecțiune nu se vindecă, tratamentul ei fiind doar simptomatic.
Sclerodermia este o afecțiune rară a țesutului conjunctiv cu patogeneză necunoscută și complexă. Aceasta poate fi împărțită în două forme
- sclerodermia localizată (morfea, sclerodermia liniară și sclerodermia în coup de sabre)
- scleroza sistemică, care poate fi clasificată, pe baza criteriilor clinice și serologice, ca scleroză sistemică limitată (cunoscută anterior ca sindrom CREST care cuprinde calcinoză, fenomene Raynaud, dismotilitate esofagiană, sclerodactilie și telangiectazie) sau scleroză sistemică difuză
Sclerodermia localizată este o boală a pielii și a țesutului subcutanat, care duce la zone de piele îngroșată. La biopsie, aceste regiuni cutanate îngroșate dezvăluie fibroză dermică similară cu modificările histopatologice observate la pielea îngroșată în scleroza sistemică. Cu toate acestea, sclerodermia localizată nu este asociată cu fenomenul Raynaud, evenimentele ischemice digitale sau cu implicarea organelor interne. Anticorpii antinucleari (ANA) pot fi prezenți în până la 50% din cazurile de sclerodermie localizată. Totuși, autoanticorpii mai specifici, cum ar fi anti-centromer, anti-SCL70 și anti-ARN polimeraza III sunt absenți. Sclerodermia localizată nu este asociată cu o mortalitate crescută.
Scleroza sistemică, pe de altă parte, este asociată cu mai multe manifestări sistemice, cu implicarea organelor interne și cu o mortalitate crescută. Clasificarea sclerozei sistemice se bazează pe afectarea pielii.
Scleroza sistemică cutanată limitată, cunoscută anterior sub numele de sindrom CREST, este asociată cu îngroșarea pielii în zona distală a coatelor și genunchilor și la nivelul feței, fără implicarea trunchiului.
Scleroza sistemică cutanată difuză este asociată cu îngroșarea pielii care poate implica zonele proximale ale coatelor și genunchilor, fața și trunchiul.
Ambele forme sunt asociate cu multiple manifestări sistemice și cu pozitivitatea autoanticorpilor. Anticorpii antinucleari (ANA) pot fi prezenți în mai mult de 90% din cazurile de scleroză sistemică și cel puțin unul dintre cei mai specifici autoanticorpi (anti-centromer, anti-SCL70 și anti-ARN polimeraza III) este prezent în până la 70% de cazuri.
Organele cel mai frecvent afectate de sclerodermia sistemică sunt pielea, tractul gastrointestinal, plămânii, rinichii, mușchii scheletici și pericardul.
Din cauza rarității sale, datele epidemiologice pentru scleroza sistemică sunt rare. Incidența estimată a acestei boli în Statele Unite este de 19,3 cazuri noi la un milion de adulți pe an. În 2003, un studiu din Quebec a raportat o prevalență de 443 de cazuri la un milion de adulți. Prevalența este mai mare în America și Australia decât în Europa și Asia. Cea mai mare prevalență (660 de cazuri la un milion de adulți) a fost observată în rândul nativilor americani din Oklahoma.
Există o predominanță generală feminină, cu un raport femei/bărbați de aproximativ 5:1. Femeile tind să dezvolte scleroza sistemică la o vârstă mai fragedă în comparație cu bărbații. Vârsta maximă de debut este între 45 și 54 de ani la femeile afro-americane și între 55 și 64 de ani la femeile europene. Boala este rară la copii și adolescenți cu vârsta sub 15 ani. Debutul bolii între 15 și 24 de ani este, de asemenea, destul de rar, cu o incidență de 21,2 la un milion la femeile afro-americane și de 11,16 la un milion la femeile europene de rasă albă. Pacienții afro-americani au un risc mai mare de a dezvolta forme mai severe de scleroză sistemică, la o vârstă mai fragedă.
Semnul distinctiv al sclerodermiei sistemice este vasculopatia proliferativă/obliterativă neinflamatoare urmată de fibroză interstițială/vasculară. Infiltratele inflamatorii perivasculare ale limfocitelor T CD4+ pot fi observate la începutul bolii, dar sunt absente în scleroza sistemică de lungă durată.
În stadiile ulterioare ale sclerozei sistemice, există fibroză perivasculară extinsă, ocluzie luminală progresivă și fibroză tisulară. Scleroza sistemică precoce este asociată cu edem dermic la nivelul pielii, iar infiltratul inflamator perivascular este compus din limfocite T și monocite. În stadiile ulterioare, predomină fibroza dermică, iar histopatologia relevă pierderea capilarelor dermice și pierderea anexelor pielii, foliculilor de păr, glandelor sudoripare și glandelor sebacee, pe lângă o expansiune dermică marcată de acumulare densă de colagen și acid hialuronic. Există o pierdere a limfaticului dermal și a stratului adipos subcutanat.
Afectarea pulmonară este foarte frecventă în scleroza sistemică, fiind asociată cu modificări inflamatorii la începutul bolii, cu fibroză și afectare vasculară mai târziu. Modificările inflamatorii precoce sunt observate în pereții alveolari, cu infiltrare cu limfocite, macrofage și celule plasmatice. Afectarea pulmonară în scleroza sistemică este reprezentată cel mai frecvent de pneumonita interstițială nespecifică. Pneumonia interstițială obișnuită, care prezintă o distribuție neregulată a fibrozei cu focare fibroblastice diseminate apare mai rar, dar are un prognostic mai rezervat. Hipertensiunea arterială pulmonară apare din cauza vasculopatiei, precum și a unei pierderi a microvasculaturii pulmonare din cauza fibrozei pulmonare progresive.
Afectarea renală a devenit mai puțin frecventă în ultima perioadă. Modificările ischemice cronice sunt frecvente, dar glomerulonefrita este mai puțin frecventă. Criza renală sclerodermică, o manifestare rară a sclerodermiei sistemice, dar care pune viața în pericol, este asociată cu modificări observate în microangiopatia trombotică sau hipertensiunea malignă.
Fibroza poate fi observată și în alte organe, inclusiv la nivelul tractului gastrointestinal, al glandei tiroide, al glandelor salivare, organelor genitale. Afectarea cardiacă poate evidenția pericardită constrictivă, fibroză/efuziuni pericardice și fibroză miocardică neregulată.
Scleroza sistemică este asociată cu o mortalitate ridicată; dintre toate tulburările vasculare de colagen, scleroza sistemică are cea mai mare mortalitate. Cea mai frecventă cauză de mortalitate a fost, în trecut, criza renală de sclerodermie, înainte de apariția inhibitorilor ECA. Utilizarea inhibitorilor ECA a scăzut mortalitatea legată de scleroza sistemică.
În prezent, cea mai frecventă cauză de mortalitate este boala pulmonară.
Prognosticul sclerozei sistemice s-a îmbunătățit semnificativ în ultimii 30 de ani. Ratele de supraviețuire la 5 ani sunt de până la 80%. Cu toate acestea, pacienții cu hipertensiune arterială pulmonară avansată au o rată de supraviețuire mai mică de 50% la 2 ani
Înainte de descoperirea inhibitorilor ECA, rata de supraviețuire la un an pentru pacienții cu criză renală sclerodermică era mai mică de 15%, dar acum, cu mai multă conștientizare și utilizarea inhibitorilor ECA, rata de supraviețuire la un an în criza renală sclerodermică este mai mare de 85%. Pacienții cu scleroză sistemică prezintă, de asemenea, un risc crescut de apariție a afecțiunilor maligne, în special a cancerului pulmonar. Riscul de adenocarcinom esofagian poate fi, de asemenea, crescut, în asociere cu refluxul gastroesofagian cronic.
Cauzele sclerozei sistemice
Etiologia exactă a bolii nu este complet înțeleasă și se consideră că atât factorii genetici, cât și factorii de mediu contribuie la dezvoltarea sclerozei sistemice.
Predispoziția genetică pare să fie limitată; totuși, se observă adesea o predispoziție familială pentru boli autoimune. Anumite modificări genetice pot influența severitatea și dezvoltarea bolii. Unele dovezi corelează scleroza sistemică cu infecția cu citomegalovirusul, virusul Epstein-Barr și parvovirusul B19, dar sunt limitate.
Unul dintre mecanismele suspectate din spatele fenomenului autoimun este existența microchimerismului, adică a celulelor fetale care circulă în sângele matern, declanșând o reacție imună la ceea ce este perceput ca material străin.
O formă distinctă de scleroză sistemică se poate dezvolta la pacienții cu insuficiență renală cronică. Această formă, numită dermopatie fibrozantă nefrogenă sau fibroză sistemică nefrogenă, a fost asociată cu expunerea la substanța de contrast care conține gadoliniu.
Bleomicina (un agent chimioterapeutic) și, posibil, chimioterapia cu taxani pot provoca sclerodermie, iar expunerea profesională la solvenți a fost legată de un risc crescut de scleroză sistemică. Expunerea la praful de silice, toluen, xilen, tricloretilenă, clorură de polivinil a fost ocazional legată de dezvoltarea sau agravarea sclerozei sistemice. Fumatul nu s-a dovedit a fi un factor de risc.
Fiziopatologia sclerozei sistemice este complexă și incomplet înțeleasă. Semnele distinctive ale bolii sunt:
(1) afectarea vasculară
(2) autoimunitatea
(3) fibroza tisulară
Leziunea vasculară inițială în scleroza sistemică poate fi declanșată de mai mulți factori, inclusiv virusuri, diferite substanțe din mediu, autoanticorpi, enzime proteolitice și citokine inflamatorii. Această afectare vasculară inițială duce la activarea celulelor endoteliale, urmată de supraexprimarea moleculelor de adeziune, ducând la activarea trombocitelor și a cascadelor trombotice și fibrinolitice. Celulele endoteliale activate eliberează, de asemenea, ET-1, un vasoconstrictor puternic și promovează aderența leucocitelor, proliferarea celulelor musculare netede vasculare și activarea fibroblastelor. Celulele endoteliale activate se transdiferențiază în celule mezenchimale cu anomalii funcționale proeminente, cum ar fi răspunsul afectat la vasodilatatoare. Trombocitele activate eliberează tromboxan-A2, PDGF și TGF-β și activează trombina, ducând la coagulare, tromboză, vasoconstricție și activarea fibroblastelor. Astfel, această leziune vasculară inițială duce, în cele din urmă, la hipoxie tisulară și stres oxidativ.
Dereglarea imună și inflamația joacă un rol crucial în patogeneza sclerozei sistemice, cu dereglarea atât a sistemului imunitar înnăscut, cât și a celui umoral. Macrofagele, monocitele și celulele dendritice activate promovează, în continuare, leziunile vasculare și fibroza prin activarea celulelor T și a celulelor B și producția de citokine pro-fibrotice și pro-inflamatorii. Autoimunitatea umorală și autoanticorpii sunt prezenți la aproape toți pacienții cu scleroză sistemică. Celulele B activate produc autoanticorpi care au un rol esenția în patogeneză, pe lângă faptul că servesc ca markeri de diagnostic.
Rezultatul leziunii vasculare și inflamației cauzate de reacțiile autoimunitare este fibroza tisulară, prin activarea și diferențierea celulelor mezenchimale, acumularea ireversibilă a matricei extracelulare, activarea necontrolată a fibroblastelor, miofibroblastele persistente, creșterea compartimentului pericit microvascular și tranziția epitelial-mezenchimală patologică.
Simptome scleroza sistemică
În 2013, Colegiul American de Reumatologie a publicat criteriile de clasificare actualizate pentru scleroza sistemică. Conform acestora, principalele simptome asociate sclerozei sistemice cuprind:
- Îngroșarea bilaterală a pielii în apropierea articulațiilor metacarpofalangiene
- Îngroșarea pielii degetelor
- Degete umflate
- Leziuni ale degetelor
- Cicatrici la vârful degetelor
- Ulcere digitale la vârf
- Telangiectazie
- Capilare anormale ale pliului unghial
- Fenomenul Raynaud
- Boală pulmonară
- Tensiune arterială pulmonară
- Anticorpi pozitivi specifici sclerozei sistemice (anticentromer, anti-Scl-70, Anti-ARN polimeraza III)
Iată care este descrierea simptomelor sclerozei sistemice:
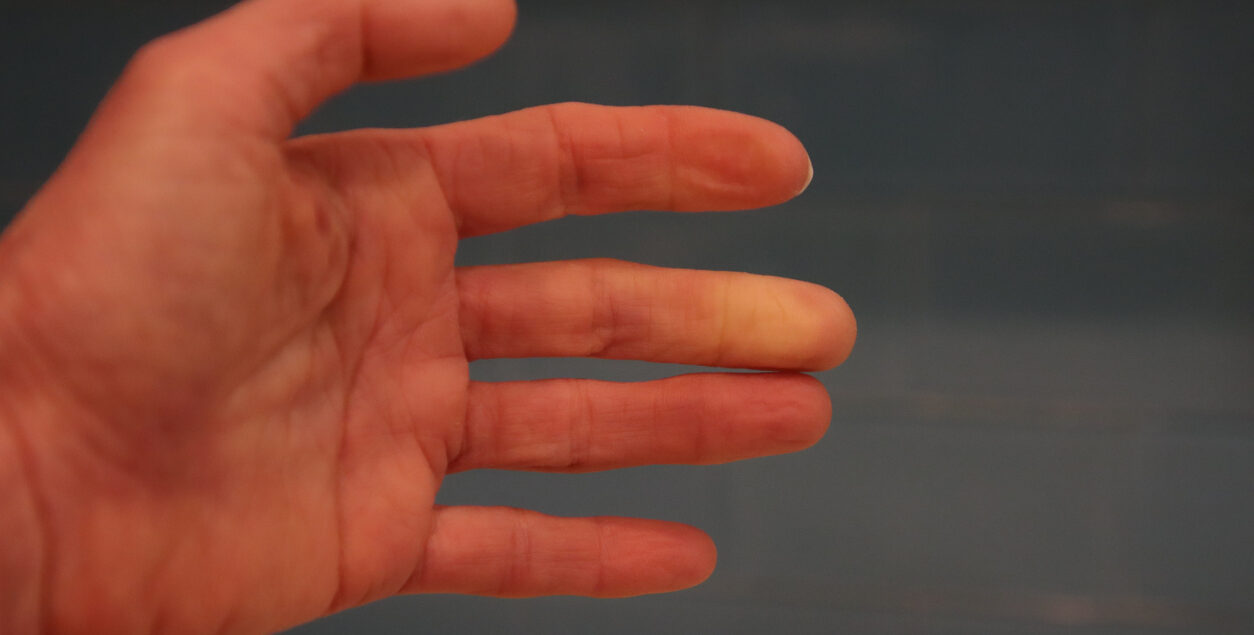
Fenomenul Raynaud
Acesta este o caracteristică precoce a sclerodermiei sistemice și este observat la peste 95% dintre pacienții cu această boală. Vasospasmul la expunerea la frig care duce la schimbarea trifazică a culorii poate fi observat la nivelul degetelor, mai frecvent la extremitățile superioare. Aceste modificări pot fi observate și la ureche, nas sau limbă. Vasospasmul duce la paloarea inițială cu decolorare albă bine delimitată, urmată de modificări ischemice cu decolorare albăstruie închisă și de hiperemie reactivă cu decolorare roșie.
Fenomenul Raynaud poate preceda cu câțiva ani implicarea viscerală, mai ales în scleroza sistemică cutanată limitată. În scleroza sistemică difuză, fenomenul Raynaud pot apărea simultan sau la scurt timp după modificările pielii.
Trebuie subliniat faptul că fenomenul Raynaud apare la până la 15% din populația generală, fără scleroză sistemică sau boli ale țesutului conjunctiv subiacente. Acesta este denumit Raynaud primar și este asociat cu o predominanță feminină, o vârstă fragedă de debut (de obicei mai puțin de 20 de ani), caracteristici clinice ușoare, simetrice, capilare normale cu pliul unghial, ANA negativ și este benign, fără complicații ischemice. Fenomenul Raynaud secundar observant în scleroza sistemică poate fi asociat cu complicații severe, precum vasculopatia subiacentă, pierderea flexibilității vaselor, ulcere digitale și pierderea țesutului vârfului degetelor, ischemie digitală și gangrenă uscată, care poate duce la amputare. Infecțiile suprapuse sunt frecvente.
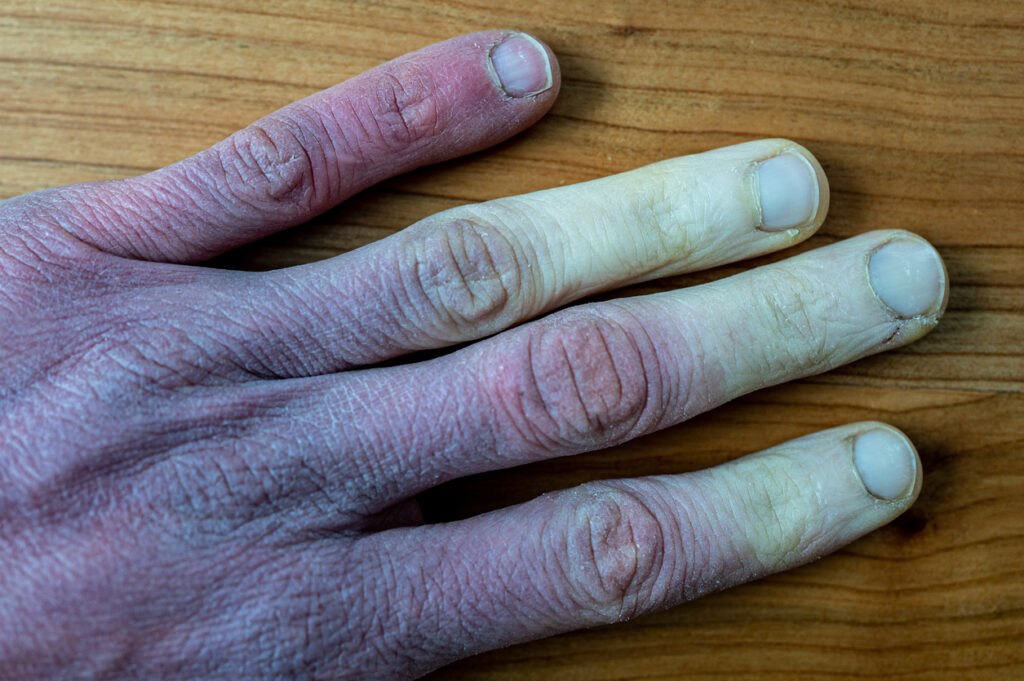
Manifestări cutanate
Implicarea pielii este cea mai evidentă caracteristică a sclerozei sistemice și este prezentă la aproape toți pacienții, cu diferite grade și severitate.
Este afectată pielea la nivelul coatelor, genunchilor, feței sau trunchiului, în funcție de tipul de scleroză sistemică.
„Faza degetului umflat” inițial este asociată cu inflamația și edemul mâinilor și poate dura câteva luni. Pruritul, durerea de tip arsură și eritemul sunt frecvente. Edemul poate duce la compresia structurilor subiacente, iar neuropatiile de compresie, cum ar fi sindromul de tunel carpian, sunt frecvente.
Pierderea anexelor pielii provoacă uscăciunea pielii. Îngroșarea pielii și fibroza încep să se dezvolte în această fază inițială, care este apoi urmată de faza fibrotică. În această a doua fază fibrotică prelungită, fibroza și îngroșarea pielii încep distal de articulațiile metacarpofalangiene (sclerodactilie) și progresează proximal.
Pielea groasă și fibroza structurilor subcutanate mai profunde duc la contracturi permanente și scăderea mobilității articulațiilor periferice. Există o pierdere suplimentară a anexelor pielii și a țesutului adipos subcutanat (lipodistrofie). Implicarea facială determină deschidere bucală mică (gura de pește sau facies mascat). Ulcerele cutanate se pot dezvolta la locurile traumatismelor, cum ar fi suprafețele extensoare ale articulațiilor metacarpofalangiene, interfalangiene sau ale cotului. Se pot observa zone de depigmentare a pielii.
Telangiectaziile (dilatații permanente ale vaselor mici de sânge situate în derm) pot fi observate în scleroza sistemică, din cauza dilatației capilarelor și sunt frecvente pe mâini, față, suprafețe mucoase și, uneori, pe trunchi. Telangiectaziile se albesc la aplicarea presiunii. Acestea pot crește în timp și sunt considerate a fi asociate cu un risc crescut de hipertensiune pulmonară.
Calcinoza subcutanată poate fi observată atât în cazul sclerozei sistemice limitate, cât și al celei difuze și la pacienții cu un anticorp anti-centromer pozitiv. Calcinoza este determinată de depunerile subcutanate de hidroxiapatită de calciu și este observată cel mai frecvent în zonele traumatice, cum ar fi degetele și suprafețele extensoare ale coatelor. Calcinoza poate duce la ulcerații ale pielii și infecții secundare.
Manifestări musculo-scheletice
Simptomele musculo-scheletice sunt observate la aproape toți pacienții cu scleroză sistemică. Artralgia și mialgia sunt frecvent prezente. Sinovita și artrita inflamatorie pot fi, de asemenea, observate și pot avea un model asemănător poliartritei reumatoide, cu implicarea articulațiilor metacarpofalangiene, interfalangiene proximale, încheieturii mâinii și gleznei. Eroziunile sunt, totuși, rare, dar pot fi observate în asociere cu calcinoza periarticulară. Implicarea articulară mare este rară, dar poate fi observată în scleroza sistemică difuză, la fel ca și resorbția osoasă distală și osteoliza ce pot apărea în stadiile târzii ale bolii.
Contracturile articulare care implică mâinile sunt frecvente. Frecarea tendoanelor din cauza inflamației, edemului și fibrozei tecii tendoanelor poate fi observată în până la 30% din cazuri.
O miopatie inflamatorie sau miozită similară cu polimiozita poate fi observată la până la 10% dintre pacienții cu scleroză sistemică și este asociată cu slăbiciune musculară proximală rapid progresivă, enzime musculare crescute și fenomene inflamatorii. Miopatia în scleroza sistemică este, de obicei, asociată cu un prognostic general prost.
În plus, pacienții cu scleroză sistemică pot prezenta o scădere a forței musculare din cauza malnutriției sau din cauza decondiționării asociate bolilor articulare și fibrozei pielii.
Manifestări gastrointestinale
Implicarea gastrointestinală este, de asemenea, aproape universală în ambele forme de scleroză sistemică. Simptomele pot varia, de la ușoare până la severe și poate fi implicat orice segment al tractului gastrointestinal.
Implicarea orofaringiană include strângerea pielii periorale și scăderea deschiderii bucale, parodontoza și gingivita. Uscarea gurii poate fi observată din cauza fibrozei glandelor salivare sau din cauza infiltratului inflamator în sindromul Sjögren secundar.
Dismotilitatea esofagiană din cauza fibrozei esofagiene, implică mai ales cele două treimi distale ale esofagului, ducând la disfagie și arsuri la stomac și este observată la până la 90% dintre pacienții cu scleroză sistemică. Sfincterul esofagian inferior devine hipoton, ceea ce agravează simptomele de reflux. Complicațiile dismotilității esofagiene pot include esofagită, stricturi esofagiene, esofagul Barrett și chiar sângerări.
Implicarea gastrică poate include golirea gastrică întârziată (gastropareză), care poate duce la sațietate precoce, balonare, greață, vomă și anorexie, ce poate provoca malnutriție și scădere în greutate.
Ectazia vasculară antrală gastrică (GAVE), cunoscută și sub denumirea de „stomacul de pepene verde”, este rezultatul telangiectaziei gastrice și poate duce la sângerări oculte sau mari de sânge.
Dismotilitatea intestinală poate provoca diaree, constipație și creșterea excesivă a bacteriilor intestinale. Telangiectaziile mucoasei pot provoca hemoragii gastrointestinale oculte. Dismotilitatea intestinală poate duce la pseudo-obstrucție care poate fi gravă.
Diverticulii cauzați de atrofia musculară a mucoasei intestinale sunt caracteristici pentru scleroza sistemică.
Scăderea tonusului sfincterului anal poate duce la prolaps rectal și incontinență.
Manifestări pulmonare
Boala pulmonară este principala cauză de mortalitate la pacienții cu scleroză sistemică. Afectarea pulmonară caracteristică include boala pulmonară interstițială și/sau hipertensiunea pulmonară. Manifestările pulmonare mai puțin frecvente includ: pleurita, boala obstructivă a căilor respiratorii, pneumonia de aspirație, hemoragia pulmonară și pneumonia de organizare criptogenă. Boala pulmonară în scleroza sistemică poate varia de la o variantă asimptomatică clinic până la insuficiență respiratorie progresivă cu morbiditate severă.
Boala pulmonară interstițială este mai frecventă și mai severă în cazul sclerozei sistemice difuze. Aceasta se dezvoltă, de obicei, în primii 4 până la 5 ani de la diagnosticul de scleroză sistemică.
Simptomele bolii pulmonare interstițiale includ dispnee, oboseală și, mai târziu, o tuse neproductivă. Testarea funcției pulmonare relevă un model restrictiv cu o scădere a volumelor pulmonare.
CT de înaltă rezoluție (HRCT) a toracelui evidențiază atenuări pulmonare subpleurale crescute în zonele bazale posterioare bilaterale. Pot fi observate opacități de sticlă șlefuită, care sugerează alveolită. Alte constatări includ structuri tip fagure de miere, bronșiectazie de tracțiune și îngroșarea septurilor interlobulare.
Hipertensiunea pulmonară este o altă manifestare frecventă în scleroza sistemică și poate varia de la boala asimptomatică la forme severe, cu insuficiență cardiacă dreaptă. Hipertensiunea arterial pulmonară apare de obicei târziu în boală, la mai mult de 10 ani după diagnosticul de scleroză sistemică. Simptomele includ inițial dispnee și dureri în piept, ulterior umflarea extremităților inferioare, amețeli și sincopă.
Manifestări cardiace
Manifestările cardiace includ pericardită, revărsat pericardic, cardiomiopatie dilatativă și aritmii. Disfuncția diastolică a ventriculului stâng poate apărea secundar hipertensiunii pulmonare. Afectarea cardiacă este asociată cu un prognostic prost. Revărsările pericardice sunt de obicei mici, exudative, iar tamponarea este mai puțin frecventă. Efuziunile pericardice sunt mai frecvente în scleroza sistemică difuză și sunt predictive pentru criza renală sclerodermică. Cardiomiopatia dilatată apare din cauza fibrozei miocardice neregulate. Fibroza căii de conducere poate duce la aritmii, cea mai frecventă constatare fiind contracțiile ventriculare premature, deși au fost raportate și blocuri cardiace, întârzieri de conducere intraventriculară și tahicardie supraventriculară.
Manifestări renale
Criza renală sclerodermică (SRC) a fost aproape întotdeauna fatală și a fost principala cauză de mortalitate în scleroza sistemică, înainte de descoperirea inhibitorilor enzimei de conversie a angiotensinei. Această manifestare este observată la aproximativ 10% dintre pacienții cu scleroză sistemică, în general forma difuză. Poate să apară în decurs de 3 ani de la diagnostic. Factorii de risc pentru dezvoltarea SRC includ rasa afro-americană, efuziunea pericardică, frecarea tendoanelor, anticorpi anti-ARN polimerază III și utilizarea de corticosteroizi în doze mari (sau chiar în doze mici de lungă durată). Caracteristicile clinice includ hipertensiunea de debut sau hipertensiunea malignă, împreună cu insuficiența renală. Din cauza microangiopatiei asociate, se întâlnesc frecvent anemie hemolitică și trombocitopenie. Proteinuria, dacă este observată, este de obicei ușoară. Hematuria microscopică este frecvent prezentă.
Alte manifestări
Hipotiroidismul este observat la până la 15% dintre pacienții cu scleroză sistemică, în special localizată și poate să apară din cauza fibrozei glandei tiroide. În plus, bolile tiroidiene autoimune (tiroidita Hashimoto și boala Graves) sunt mai frecvente la pacienții cu scleroză sistemică.
Pacienții cu scleroză sistemică prezintă un risc crescut pentru alte boli autoimune, cum ar fi ciroza biliară primară și sindromul Sjögren secundar. Sindroamele de suprapunere sunt frecvente și pot include o suprapunere a sclerozei sistemice cu artrita reumatoidă și polimiozită.
Pacienții cu scleroză sistemică prezintă, de asemenea, un risc crescut de tulburări psihologice, cum ar fi depresia, care este observată la până la 50% dintre cazuri.
Complicațiile sclerozei sistemice
Scleroza sistemică este asociată cu multiple complicații, în mare parte secundare leziunilor organelor cauzate de fibroză. Ischemia digitală poate duce la cangrenă care necesită amputare. Implicarea gastrointestinală poate duce la malnutriție. Afectarea pulmonară este cauza principală de morbiditate la pacienții cu scleroză sistemică, ducând la fibroză pulmonară permanentă. Bolnavii cu criză renală sclerodermică pot avea leziuni renale permanente, deși, cu inhibitori ai ECA, funcția renală se recuperează la majoritatea acestor pacienți.
Diagnosticul sclerodermiei sistemice
Diagnosticul de scleroză sistemică este un diagnostic clinic care necesită numeroase investigații. Detectarea precoce a bolii este crucială în abordarea pacienților cu scleroză sistemică. Etapele diagnostice cuprind:
Evaluarea clinică
Grosimea pielii va fi evaluată prin scorul modificat al pielii Rodnan, care dă scoruri de la 0 la 3, 0 pentru zonele neafectate și 3 pentru îngroșarea severă a pielii. Examenul capilar al pliului unghial va fi efectuat la toți pacienții cu fenomen Raynaud cu suspiciune de scleroză sistemică.
Examenul fizic multisistemic va fi efectuat la fiecare vizită, pentru a evalua implicarea organelor de bază. Monitorizarea atentă a tensiunii arteriale atât în clinică, cât și la domiciliu este recomandată cu tărie, în special la pacienții cu un diagnostic recent de scleroză sistemică asociată cu hipertensiune arterială de debut. Agravarea semnificativă a hipertensiunii inițiale poate fi un indicator al crizei renale sclerodermice.
Testele de autoanticorpi
Autoanticorpii servesc ca un instrument important de diagnostic, dar au și valoare prognostică și pot prezice fenotipul bolii și evoluția ei.
Anticorpul antinuclear (ANA) se măsoară prin imunofluorescență directă și este pozitiv în mai mult de 90% din cazurile de scleroză sistemică. La pacienții care sunt negativi pentru ANA, alte diagnostice diferențiale vor fi excluse, înainte de confirmarea diagnosticului de scleroză sistemică.
Anticorpii anti-centromer vizează 4 antigene centromerice și sunt observați în scleroza sistemică localizată și foarte rar în forma difuză. Acești anticorpi pot fi observați și în sindromul Sjögren și lupusul eritematos sistemic. Anticorpii anti-centromeri sunt asociați cu un risc crescut de hipertensiune arterială pulmonară. Ei sunt, de asemenea, asociați cu implicarea cutanată limitată, risc mai scăzut de boală pulmonară interstițială și supraviețuire generală mai bună în comparație cu ceilalți autoanticorpi.
Anticorpii anti-topoizomeraza I (Scl-70) vizează regiunea catalitică a ADN helicazei topoizomerazei I. Anticorpii anti-SCL-70 sunt observați în forma difuză a sclerozei sistemice și rar în forma localizată. Anticorpii anti-SCL-70 sunt asociați cu un risc crescut de afectare cutanată difuză, boală pulmonară interstițială și implicare cardiacă.
Anticorpii anti-ARN polimerază III vizează ARN polimeraza III eucariotă. Aceștia sunt mai specifici pentru scleroza sistemică difuză și sunt asociați cu o evoluție rapidă și o implicare difuză agresivă a pielii, rezultate cutanate slabe și criză renală de sclerodermie. Anticorpii anti-ARN polimerază III sunt, de asemenea, asociați cu un risc mai scăzut de boală pulmonară interstițială și hipertensiune pulmonară. Unele studii au indicat o asociere de afecțiuni maligne la pacienții cu test pozitiv de anticorpi anti-ARN polimerază III.
Anticorpii anti-U3-RNP (fibrilarină) sunt prezenți mai mult la pacienții afro-americani și sunt asociați cu un prognostic general prost, afectare mai mare a organelor interne, afectare cutanată difuză, boală pulmonară interstițială, hipertensiune arterială pulmonară, criză renală sclerodermică, miozită/miopatie și implicare cardiacă.
Alți autoanticorpi
Anticorpii anti-Th/To sunt asociați cu o boală limitată a pielii.
Anticorpii anti-PM/Scl sunt asociați cu boli limitate ale pielii și sindrom de suprapunere cu un risc mai mare de miozită inflamatorie și boală pulmonară interstițială.
Anticorpii anti-U1-RNP sunt mai frecventi la afro-americani și sunt asociați cu sindromul de suprapunere și boala mixtă a țesutului conjunctiv cu afectare cutanată limitată și risc mai mare de artrită inflamatorie, miozită, erupții cutanate cu lupus și nefrită lupică.
Anticorpii anti-Ku sunt, de asemenea, asociați cu sindromul de suprapunere în scleroza sistemică, precum și cu artrită inflamatorie și miozită.
Evaluarea de laborator
Analizele recomandate includ:
- hemoleucograma completă pentru a verifica dacă există anemie care poate fi multifactorială.
- dozarea creatininei și ureei, pentru a evalua funcția renală
- markerii inflamatori: o creștere semnificativă a acestor markeri poate fi observată la pacienții cu miopatie inflamatorie activă sau artrită inflamatorie.
- enzimele musculare, inclusiv creatinkinaza și aldolaza, pot fi crescute mai ales atunci când este prezentă miopatia inflamatorie.
Evaluare auxiliară și radiografică
Radiografia extremităților pot evidenția calcinoza și pierderea falangei distale. Eroziunile periarticulare sunt rare și mai puțin frecvente, deși se poate observa osteopenia periarticulară.
Ecografia musculo-scheletică poate arăta caracteristici ale tenosinovitei.
Când se suspectează implicarea musculară, electromiograma/testul vitezei de conducere nervoasă este testul inițial de elecție și, dacă este anormal, va fi urmat de o biopsie musculară.
Modalitatea imagistică de elecție pentru evaluarea bolii pulmonare interstițiale este o scanare CT de înaltă rezoluție, deoarece radiografia toracică nu evidențiază modificările subtile.
Ecocardiografia transtoracică se face de obicei inițial când se suspectează hipertensiune arterială pulmonară, deși trebuie urmat cateterismul cardiac drept pentru a confirma diagnosticul și pentru a exclude alte etiologii.
Electrocardiografia și monitorul Holter pot fi utile în depistarea aritmiilor.
Efuziunile pericardice pot fi bine vizualizate pe ecocardiografia transtoracică.
RMN cardiac poate fi necesar la pacienții la care se suspectează implicarea miocardică.
Endoscopia gastrointestinală superioară, manometria esofagiană, studiile de deglutiție cu bariu și sonda de pH de 24 de ore pot fi utilizate atunci când se suspectează afectarea esofagiană și implicarea gastrointestinală superioară. Dismotilitatea esofagiană, care duce la un esofag dilatat cu descoperirea imagistică a aerului excesiv în esofag, este o constatare caracteristică care poate fi observată pe o scanare CT.
Testarea funcției pulmonare
Testele funcției pulmonare, inclusiv spirometria, volumele pulmonare și capacitatea de difuzie, pot detecta un model restrictive timpuriu în boala pulmonară interstițială.
Tratamentul în caz de scleroză sistemică
Scleroza sistemică este o boală gravă, cu multiple implicații în viața pacienților, care poate duce la dizabilitate severă. Boala nu are vindecare și este disponibil doar un tratament simptomatic.
Scleroza sistemică poate afecta mai multe organe și, prin urmare, se recomandă o abordare interprofesională, incluzând: medicul de familie, reumatologi, gastroenterologi, cardiologi, pneumologi, nefrologi și dermatologi.Toți pacienții cu sclerodermie sistemică trebuie monitorizați îndeaproape. Echipa de asistență medicală joacă un rol crucial în educarea pacientului și în monitorizarea și urmărirea atentă. Educația pacientului include încurajarea de a se implica în exerciții regulate, alimentație sănătoasă și stil de viață activ, precum și sprijin emoțional și asistare psihologică.
”Tratamentele ajută la ameliorarea simptomelor și poate modifică rezultatul bolii, mai ales la începutul evoluției. Se concentrează pe suprimarea inflamației și dilatarea vaselor de sânge anormale/îngustate. Unele tratamente mai noi vizează cai imunologice specifice și molecule de semnalizare. Tratamentul este complex și include: terapii sistemice, vasodilatatoare, tratamentul manifestărilor cutanate, măsuri generale, cum ar fi menținerea căldurii corpului (pentru prevenirea fenomenului Raynaud), exerciții de întindere pentru articulații pentru a reduce riscul agravării contracturilor și microstomiei și fizioterapia specifică, profilaxia și tratamentul ulcerului, tratamentul afecțiunilor gastrointestinale și renale.”, precizează kinetoterapeutul Cristian Dumitrescu pe site-ul centrokinetic.ro
Diagnosticul precoce este o strategie cheie pentru ameliorarea unora dintre simptomele sclerozei sistemice. Evaluarea clinică și identificarea organelor afectate, precum și monitorizarea progresiei bolii sunt esențiale pentru eficacitatea tratamentului. În plus, este important ca obiectivele tratamentului să fie holistice și adaptate pentru optimizarea calității vieții pacienților afectați, pe lângă prevenirea leziunilor suplimentare ale organelor.
Mai mulți agenți medicamentoși au fost studiați pentru diferite manifestări ale sclerozei sistemice, deși sunt necesare cercetări suplimentare pentru confirmarea lor. Printre agenţii imunosupresori cei mai des utilizaţi se numără:
- ciclofosfamida (boală pulmonară, boală de piele)
- micofenolat mofetil (boală pulmonară, boală de piele)
- metotrexat (boală de piele, artrită inflamatorie, miozită)
- azatioprină (boală de piele, boală pulmonară, miozită)
- hidroxiclorochina (boală de piele)
- ciclosporina (boală de piele)
- infliximab (artrita inflamatorie)
- rituximab (boală de piele, boli pulmonare)
Corticosteroizii sunt, în general, evitați în scleroza sistemică. Corticosteroizii în doze mari și chiar utilizarea pe termen lung a corticosteroizilor în doze mici până la moderate au fost asociați cu precipitarea crizei renale de sclerodermie.
Dacă este absolut necesar, trebuie utilizați în cea mai mică doză, pentru cel mai mic timp posibil cum ar fi în cazul miozitei inflamatorii, artritei inflamatorii refractară și/sau activă.
Terapii specifice în sclerodermie
Fenomenul Raynaud
Scopul tratamentului în cazul fenomenului Raynaud este de a preveni ischemia digitală și ulcerul. Aceste ulcere ischemice sunt mult mai ușor de prevenit decât de tratat. Pacienții trebuie să mențină extremitățile și corpul cald, să evite fumatul, stresul și să elimine medicamentele simpatomimetice atunci când este posibil. La pacienţii trataţi cu beta-blocante, trebuie făcută o încercare de a trece la alt medicament, dacă este posibil, deoarece beta-blocantele pot agrava fenomenul Raynaud.
Terapia vasodilatatoare s-a dovedit a fi eficientă în sindromul Raynaud. Agenții de primă linie sunt blocanții canalelor de calciu dihidropiridină, cum ar fi nifedipina sau amlodipina.
Pot fi luate în considerare și alte vasodilatatoare precum pentoxifilina, nitroglicerina, inhibitorii fosfodiesterazei (sildenafil).
Analogii de prostaciclină (iloprost) și antagoniștii receptorilor de endotelină (bosentan) pot fi utilizați pentru cazurile refractare cu ulcere ischemice digitale.
Simpatectomia proximală/distală poate fi luată în considerare în cazurile refractare.
Injecțiile cu toxină botulină s-au dovedit a fi eficiente în unele studii mici, deși eficacitatea este încă limitată.
Pompele vasodilatatoare pot fi utilizate la pacienții care nu pot tolera terapiile vasodilatatoare. Îngrijirea adecvată a rănilor este crucială în gestionarea pacienților cu ulcer digital.
Tratamentul bolii de piele
Mai mulți agenți imunosupresori au fost utilizați în sclerodactilie, inclusiv metotrexat, hidroxiclorochină, micofenolat de mofetil și ciclofosfamidă. Deși nu sunt date suficiente, micofenolatul de mofetil este agentul preferat de majoritatea reumatologilor în cazul îngroșării moderate până la severe a pielii.
Antihistaminicele și agenții de hidratare topici pot ameliora pruritul.
Telangiectaziile nu necesită, de obicei, nici un tratament, deși terapia cu laser poate fi luată în considerare în scopuri cosmetice.
Niciun tratament medical nu s-a dovedit a fi eficient în calcinoză, deși debulkingul chirurgical poate oferi o oarecare ameliorare în cazurile severe.
Implicarea musculo-scheletală
Majoritatea pacienților au artralgii ușoare care nu necesită tratament special sau răspund bine la medicamentele antiinflamatoare nesteroidiene.
Artrita inflamatorie poate fi tratată cu medicamente antireumatice, cum ar fi hidroxiclorochina, metotrexat. Agenții anti-TNF pot fi utilizați în artrita inflamatorie severă refractară.
Terapia fizică și ocupațională este crucială în prevenirea contracturilor.
Tratamentul miozitei inflamatorii este similar cu cel al polimiozitei, deși se vor evita corticosteroizii în doze mari.
Agenții imunosupresori precum metotrexatul și azatioprina sunt eficienți în gestionarea miozitei inflamatorii.
Managementul miopatiei neinflamatorii în scleroza multiplă este dificil, iar kinetoterapia și exercițiile sunt mai benefice decât agenții imunosupresori.
Afectarea pulmonară
Implicarea pulmonară în sleroza sistemică este acum principala cauză de mortalitate. Managementul necesită implicare interprofesională, inclusiv reumatologi, pneumologi și cardiologi.
Boala pulmonară interstițială: detectarea și gestionarea precoce pot fi esențiale și gestionarea bolii pulmonare interstițiale în scleroza sistemică.
Ciclofosfamida a fost studiată și a arătat beneficii până la 18 luni, dar beneficiul a fost pierdut la 24 de luni. Au existat studii care demonstrează eficacitatea ciclofosfamidei urmată de azatioprină pentru întreținere.
Micofenolatul de mofetil s-a dovedit, de asemenea, util.
Nintedanib, un inhibitor al tirozin kinazei, a fost aprobat de FDA pentru gestionarea bolii pulmonare interstițiale în scleroza sistemică în 2019, deoarece studiile clinice asupra acestuia au arătat o încetinire a declinului testului funcției pulmonare la pacienții cu cu boală pulmonară interstițială. Alte modalități de investigare includ transplanturile de celule stem și agenții antifibrotici. Transplantul pulmonar poate fi necesar la unii pacienți, atent selectați.
Hipertensiunea arterială pulmonară
Pe lângă educarea pacientului, stilul de viață sănătos și exercițiile fizice, poate fi recomandată oxigenoterapia, precum și diureticele și anticoagulantele.
Terapia vasodilatatoare este recomandată și poate include inhibitori de fosfodiesterază 5 (tadalafil, sildenafil), antagoniști ai receptorilor endotelinei (bosentan, sitaxsentan, ambrisentan, macitentan) și/sau analogi ai prostaciclinei (epoprostenol, treprostinil, beraprost, iloprost). Terapia cu prostaciclină este considerată a fi cea mai eficientă.
Terapia combinată poate fi luată în considerare la pacienții care nu reușesc să se amelioreze la monoterapie sau care au hipertensiune arterială pulmonară severă.
Implicarea cardiacă
Managementul aritmiilor include agenți antiaritmici și, uneori, folosirea unui stimulator cardiac. Până în prezent, nu există dovezi ale eficacității agenților imunosupresori sau terapiei cu vasodilatatoare în implicarea cardiacă legată de sclerodermia sistemică.
Implicarea gastrointestinală
Pastilele fără zahăr și stimulatorii secreției salivare, precum pilocarpina sau cevimelina pot fi folosiți pentru a preveni uscarea gurii.
La pacienții cu arsuri la stomac și reflux gastroesofagian se recomandă modificarea stilului de viață și a dietei, evitarea meselor târzii și mari și evitarea alimentelor picante, precum și consumul de mese mici și frecvente.
Inhibitorii pompei de protoni sunt recomandați față de blocanții H2 și pot fi utilizate doze mari de inhibitori ai pompei de protoni, în special la pacienții cu esofagită erozivă.
În cazuri severe, poate fi luată în considerare o combinație de inhibitori ai pompei de protoni cu blocanți H2.
Pacienții cu gastropareză pot beneficia de agenți de motilitate, cum ar fi metoclopramida. Coagularea cu laser trebuie luată în considerare la pacienții cu sângerare secundară ectaziei vasculare antrale gastrice.
Pacienții cu sindrom de supracreștere bacteriană a intestinului subțire pot avea nevoie de antibiotic.
Criza renală de sclerodermie
Inhibitorii enzimei de conversie a angiotensinei (ECA) sunt singurul tratament eficient pentru criza renală sclerodermică. Aceștia trebuie administrați de la cele mai timpurii semne de scleroză sistemică și trebuie utilizată doza maximă tolerată.
Captopril, un inhibitor ECA cu acțiune mai scurtă, este preferat datorită flexibilității dozării sale, deși poate fi utilizat orice inhibitor ECA.
Nu există date privind eficacitatea blocanților receptorilor de angiotensină și a inhibitorilor de renină în criza renală sclerodermică.
Funcția renală poate continua să scadă inițial; cu toate acestea, inhibitorul ECA trebuie continuat. Când este gestionată corespunzător, funcția renală se poate îmbunătăți considerabil, deși poate dura câteva luni până la ani, permițând întreruperea dializei. Utilizarea profilactică a inhibitorilor ECA nu previne criza renală de sclerodermie și nu este recomandată, fiind asociată cu morbiditate și mortalitate crescute.
Surse:
- https://raportuldegarda.ro/sclerodermia-boala-autoimuna-rara-afectare-intreg-organism/
- https://centrokinetic.ro/servicii/reumatologie/scleroza-sistemica
- https://www.medlife.ro/glosar-medical/afectiuni-medicale/scleroza-sistemica-cauze-simptome-tratament
- https://www.medicover.ro/despre-sanatate/sclerodermie-manifestari-clinice-si-diagnostic,714,n,295
- https://www.ncbi.nlm.nih.gov/books/NBK430875/
- https://en.wikipedia.org/wiki/Systemic_scleroderma
- https://www.mayoclinic.org/diseases-conditions/scleroderma/symptoms-causes/syc-20351952
- https://www.healthline.com/health/scleroderma#outlook